近红外光控自由基聚合的独特优势,主要源于近红外光所具有的深层组织穿透能力、低散射效应与卓越的生物相容性。然而,其实际应用一直受到聚合效率低和难以获得高分子量聚合物的限制。酶级联催化和光酶催化虽有所进展,但仍存在空间分离导致的效率低或依赖短波长光源等问题,制约了其进一步发展。针对上述问题,安泽胜教授团队构筑了一种新型的超分子近红外光酶(SNIRPE)催化体系,并将其应用于近红外光催化的可控自由基聚合。仅需50 ppb的近红外光催化剂即可制备分子量高达100万g/mol以上的超高分子量聚合物。
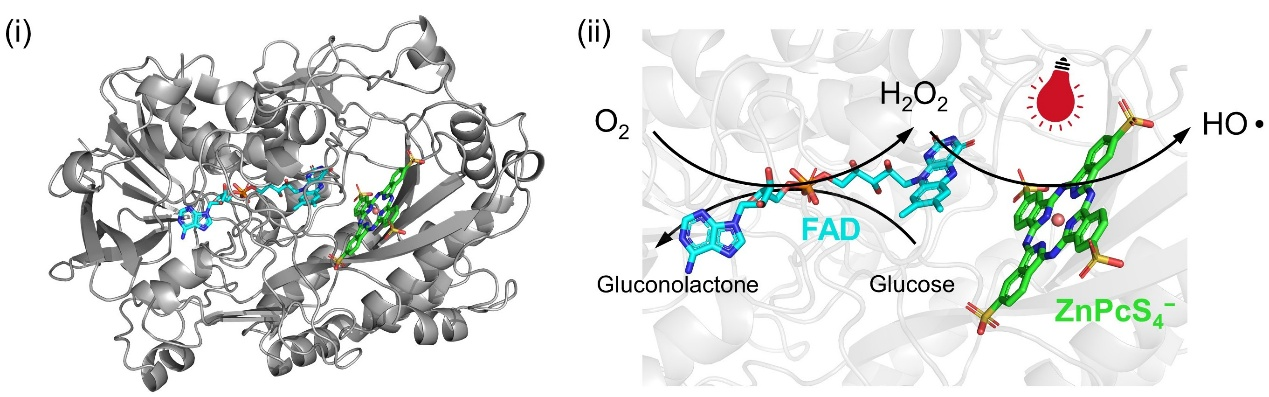
图1. SNIRPE(i)及其催化机理(ii)
什么是SNIRPE?
SNIRPE(Supramolecular NIR Photoenzyme)是一种由葡萄糖氧化酶(GOx)和四磺酸锌酞菁(ZnPcS4−)通过非共价作用自组装而成的超分子光酶系统。GOx的氨基酸残基(如Arg93、Arg333、Tyr66等)与近红外光催化剂ZnPcS4−的磺酸基和中心金属Zn存在多重非共价相互作用,这使得ZnPcS4−自发地自组装到GOx的空腔口。GOx对ZnPcS4−的限域作用,形成了内置的级联。其中,GOx除氧产生的H2O2可立即被ZnPcS4−光敏化为羟基自由基,然后可以引发可逆加成-断裂链转移(RAFT)聚合。
SNIRPE催化引发的RAFT聚合有如下特点:
高通量、规模化兼容:反应体系可从微升级放大至百毫升级,适合多种聚合实施方式(溶液、乳液、分散聚合)。
超高分子量聚合物:可制备分子量超过100万g/mol的聚合物,且结构精准、分散度低。
极低催化剂用量:仅需50 ppb的ZnPcS4−即可驱动聚合,催化剂用量远低于(3-4个数量级)现有的近红外光控自由基聚合体系。
优异的生物相容性与穿透性:近红外光可穿透5毫米厚的猪皮组织,实现“隔空聚合”,具备生物医学应用潜力。
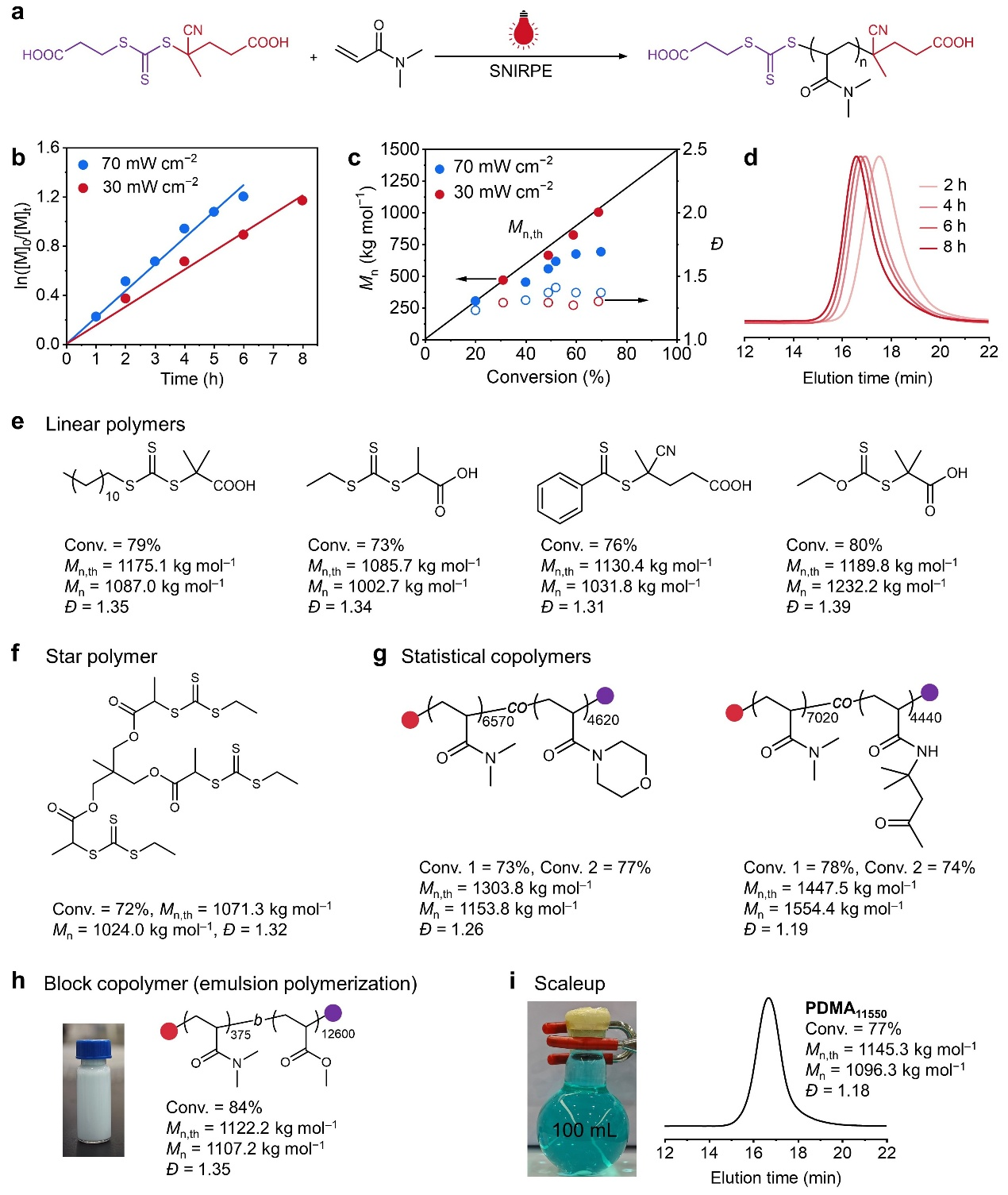
图2.SNIRPE催化引发的RAFT聚合可高通量制备超高分子量聚合物
综上所述,SNIRPE系统通过将酶催化与光催化巧妙结合,在极低催化剂用量下实现了对超高分子量聚合物的精准合成,解决了近红外光控聚合中长期存在的效率低和分子量受限的难题。未来,这一非共价设计的超分子光酶平台还有望拓展至更多酶-光敏剂组合,推动协同催化在合成化学与生物医学中的深度融合。相关论文以“Near-Infrared Photoenzymatic Catalysis at ppb Levels Enables Ultrahigh-Molecular-Weight Polymers”为题,发表在Journal of the American Chemical Society上。研究组李若雨博士为第一作者,安泽胜教授为通讯作者。相关内容已申请中国发明专利(申请号:202311286340.0)。
论文链接://pubs.acs.org/doi/10.1021/jacs.5c11130